LADICIM colabora con Valdecilla y el IDIVAL para prevenir el fallo estructural del corazón y el esqueleto
Investigadores de la Universidad de Cantabria forjan una alianza con especialistas clínicos para trasladar las estrictas metodologías de fatiga de materiales al tejido vivo y transformar el tratamiento de las patologías valvulares y óseas
Las leyes de la mecánica no distinguen entre la imponente estructura de un viaducto y la intrincada anatomía humana. Un fémur soporta cargas cíclicas de flexión de forma casi idéntica a como lo hace un pilar de hormigón. Las válvulas del corazón dependen de un tejido que se tensa y relaja millones de veces, emulando el comportamiento a fatiga de un cableado de acero de alta resistencia. Partiendo de esta equivalencia física, investigadores del Laboratorio de la División de Ciencia e Ingeniería de los Materiales (LADICIM) de la Universidad de Cantabria han consolidado una línea de trabajo junto a equipos médicos del Hospital Universitario Marqués de Valdecilla (HUMV) y del Instituto de Investigación Marqués de Valdecilla (IDIVAL). El objetivo es aplicar la ciencia de fractura de materiales al entorno biológico para descifrar, y eventualmente predecir, el colapso de los tejidos humanos.
Esta sinergia, que comenzó hace más de 15 años al amparo de un proyecto del Plan Nacional de Investigación para estudiar el comportamiento cardiovascular, ha madurado hasta forjar un auténtico ecosistema de investigación traslacional multidisciplinar. Hoy, cardiólogos, traumatólogos y científicos de Materiales comparten microscopios, máquinas de tracción y modelos de inteligencia artificial en una búsqueda conjunta de respuestas que ninguna de sus disciplinas podría hallar de forma aislada.
Curiosamente, el primer escollo a superar en esta colaboración no fue de índole tecnológica, sino comunicativa. Los campos de la ingeniería de materiales y la medicina clínica emplean nomenclaturas drásticamente distintas y abordan la resolución de problemas desde filosofías casi opuestas. «Al principio, la comunicación fue muy complicada por una cuestión lingüística. Como es obvio, en especialidades diferentes se usan lenguajes distintos y siempre se requiere un tiempo para adaptarse», explica Diego Ferreño, catedrático de la Universidad de Cantabria e investigador de LADICIM. “La necesidad de derribar ese muro nos llevó a organizar cursos de verano conjuntos en Santander y Burgos. Allí, fuera de la urgencia del laboratorio o el quirófano, se sentaron las bases de un vocabulario común”.

Por encima incluso del lenguaje latía una discrepancia profunda respecto al propio material de estudio. El metal o el polímero, una vez fabricados, inician un proceso irreversible de desgaste. La biología, en cambio, está viva. «Los organismos vivos no se comportan como los objetos inertes», recalca el profesor Ferreño. «La evolución por selección natural nos ha dotado de mecanismos de reparación que rara vez se producen en la naturaleza inerte. Y eso cambia las reglas del juego. Yo, personalmente, he aprendido mucho trabajando con los médicos».
La convergencia física de ambas disciplinas generó estampas inusuales que ya son parte del anecdotario del grupo. El doctor José Manuel Revuelta, Profesor Emérito y Catedrático de Cirugía Cardiovascular del HUMV, recuerda con exactitud su primer contacto con el entorno de los ingenieros: «Nunca olvidaré la mañana que llegué a uno de los laboratorios del LADICIM, lleno de raíles de tren que se estaban testando en grandes aparatos… y yo llevaba un frasco que contenía un corazón».
Dinámica del colapso en la válvula mitral
Uno de los pilares de esta investigación conjunta se ha centrado en desentrañar la mecánica de la válvula mitral. Para comprender su importancia, se trata de una especie de compuerta de seguridad unidireccional situada en el lado izquierdo del corazón. Su función es abrirse para dejar pasar la sangre rica en oxígeno y, acto seguido, cerrarse herméticamente cuando el corazón bombea con fuerza, evitando así que el flujo retroceda hacia los pulmones.
Con una esperanza de vida cada vez mayor, el envejecimiento de estos tejidos se ha convertido en un auténtico reto. Diversas enfermedades deterioran progresivamente las valvas (las «puertas» de esta compuerta) y, de forma crítica, las cuerdas tendinosas, los diminutos «cables» que anclan la válvula al músculo papilar, evitando que se dé la vuelta como un paraguas frente a un vendaval. Cuando estas cuerdas se elongan o se rompen, la sangre fluye hacia atrás, produciendo una insuficiencia mitral severa que merma drásticamente la capacidad respiratoria y física del paciente.
Para comprender la física de estas roturas, los investigadores de LADICIM, liderados por los catedráticos José Antonio Casado e Isidro Carrascal, decidieron someter a las cuerdas humanas, extraídas durante cirugías de reparación, a ensayos de tracción cuasiestáticos. No fue un proceso trivial. Requirió el diseño de mordazas milimétricas impresas en 3D para sujetar el tejido sin aplastarlo, y la inmersión constante de las muestras en una solución de Hanks a 37 ºC para replicar la temperatura y la composición química de la sangre humana.
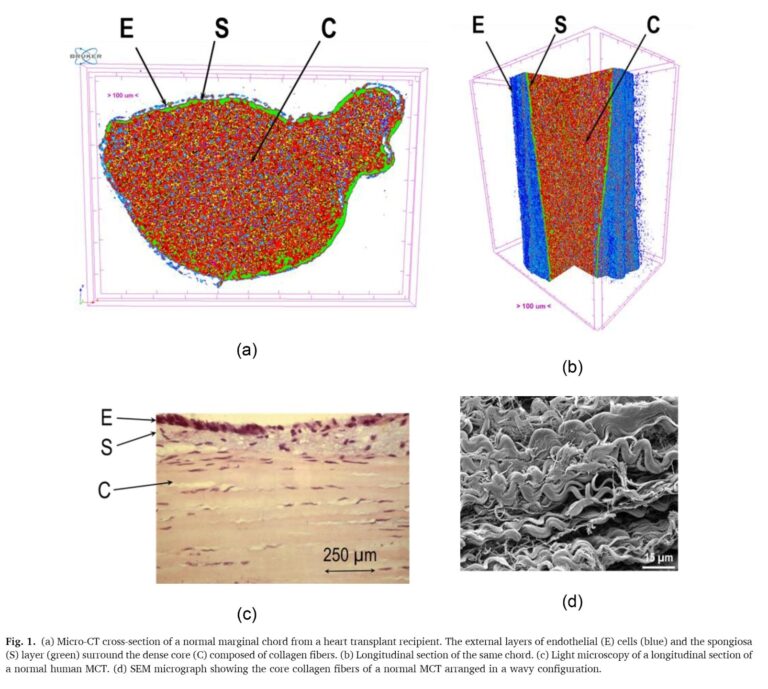
Los datos obtenidos revelaron una merma dramática de las capacidades estructurales a causa de la calcificación [1]. Mientras que una cuerda funcional extraída de un donante sano soporta tensiones con un módulo de Young de 233 MPa —una medida que define la rigidez del material; es decir, cuánta fuerza es capaz de aguantar al estirarse o deformarse—, las cuerdas moderadamente calcificadas caían desplomadas a apenas 43 MPa. En términos prácticos, el tejido enfermo pierde hasta cinco veces su rigidez natural (se vuelve más «quebradizo» y menos elástico) y su resistencia a la tracción se desploma de los 46 MPa a unos escasos 10 MPa.
«Nuestra aportación desde el campo de la ciencia de los materiales y de la ingeniería estructural ha sido fundamentalmente metodológica», precisa el profesor Ferreño. «Los médicos no son ajenos al hecho de que los tejidos experimentan fallos estructurales, pero no disponían de métodos experimentales diseñados para cuantificar e interpretar con rigor la resistencia mecánica de un componente».
Gracias al microscopio electrónico de barrido (SEM), los investigadores de LADICIM visualizaron el desastre a nivel microestructural. En un tejido sano, las fibras de colágeno exhiben un elegante patrón ondulado que les permite absorber impactos iniciales antes de tensarse. En las cuerdas calcificadas, los depósitos de hidroxiapatita obligan a estas fibras a rectificarse permanentemente, agrupándose en haces rígidos y frágiles que se fracturan de forma abrupta ante cualquier sobrecarga hemodinámica.
Inteligencia artificial para ver lo invisible
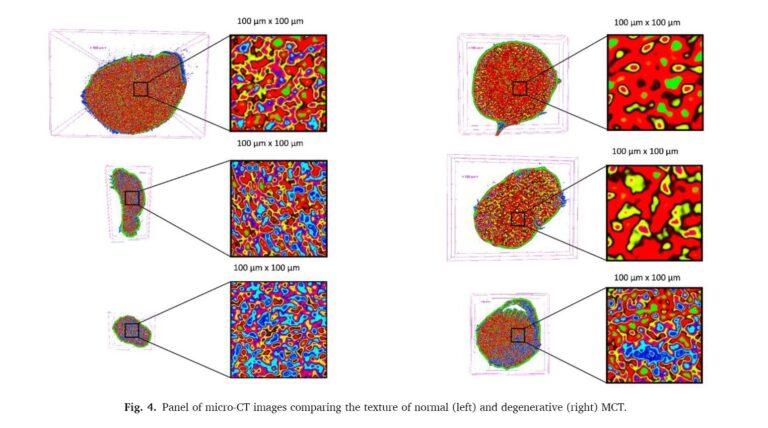
Lejos de conformarse con las pruebas destructivas, el equipo dio un salto cualitativo al incorporar la Microtomografía Computarizada (MicroTAC)combinada con aprendizaje automático (Machine Learning). El problema a resolver era de máxima urgencia en el quirófano: al reparar una válvula mitral, el cirujano observa cuerdas que parecen completamente sanas a simple vista, pero que podrían albergar ya el inicio de la enfermedad degenerativa, lo que compromete el éxito de la operación a largo plazo.
Para «ver» lo que el ojo humano ignora, los investigadores escanearon 43 cuerdas marginales humanas a una resolución de 2 micrómetros (unas 40 veces más fino que un cabello humano). Esto permite realizar un viaje virtual por el interior del tejido sin dañarlo, obteniendo miles de cortes digitales de su estructura íntima. Sobre este inmenso mapa de datos, aplicaron el algoritmo K-means, una herramienta de inteligencia artificial que agrupa los puntos de la imagen de forma automática según su densidad, identificando patrones que serían imposibles de detectar a simple vista.
Para cuantificar este daño invisible, recurrieron a la entropía de Shannon. La entropía mide el nivel de «desorden» de un sistema. Si el tejido sano es como una tela perfectamente tejida y estructurada, el tejido enfermo parece un ovillo enredado y caótico. Los resultados, publicados en 2022 en la revista Medical Engineering and Physics [2], demostraron de forma concluyente que las cuerdas enfermas presentan niveles de entropía —es decir, de caos interno— significativamente mayores. Gracias a este modelo matemático, el sistema pudo diferenciar entre el tejido sano y el degenerado con un nivel de precisión estadística casi absoluto, detectando el desorden del colágeno mucho antes de que el cirujano pueda palpar la debilidad del tejido.

En la práctica clínica, este descubrimiento permite a los médicos utilizar la entropía como una suerte de biopsia digital predictiva. Al asignar un valor numérico al desorden del tejido, el cirujano ya no tiene que fiarse solo de su intuición. Si el análisis detecta un nivel de entropía elevado, los médicos saben que esa cuerda, aunque parezca robusta en ese momento, está predestinada a romperse a corto plazo. Esto permite tomar la decisión de sustituirla preventivamente durante la operación, evitando que el paciente sufra una recaída meses después y tenga que volver a pasar por una cirugía de alto riesgo.
Ingeniería estructural aplicada a la ortopedia
El rigor analítico de estos ensayos liderados por LADICIM no tardó en expandirse hacia la traumatología, trabajando codo con codo con el Grupo de Metabolismo Óseo y Mineral del IDIVAL. Dirigido por el doctor José Antonio Riancho, Catedrático de Medicina Interna del HUMV, este equipo buscaba soluciones para la pseudoartrosis: fracturas que, por diversos motivos, se niegan a soldar y dejan al paciente en un estado de invalidez dolorosa.
Para encontrar el tratamiento más eficaz, los investigadores testaron dos fármacos. «El objetivo final era potenciar los procesos de consolidación de las fracturas, especialmente en aquellos pacientes que presentan retrasos en la curación», anota el doctor Riancho. Para ello, el equipo comparó una hormona clásica (PTH) con el ranelato de estroncio (SrR), trabajando con un modelo animal de ratones.
La respuesta definitiva no vino de una simple radiografía, sino de someter a los huesos a una auténtica prueba de fuego en la máquina de ensayos de los ingenieros [3]. Los resultados fueron contundentes: el grupo tratado con ranelato de estroncio consiguió forjar un puente óseo tan robusto que soportó una fuerza de 61 Newtons, triplicando literalmente la resistencia de los huesos que no recibieron tratamiento. La ingeniería demostraba, con números innegables, qué medicina estaba construyendo el andamiaje más fuerte.
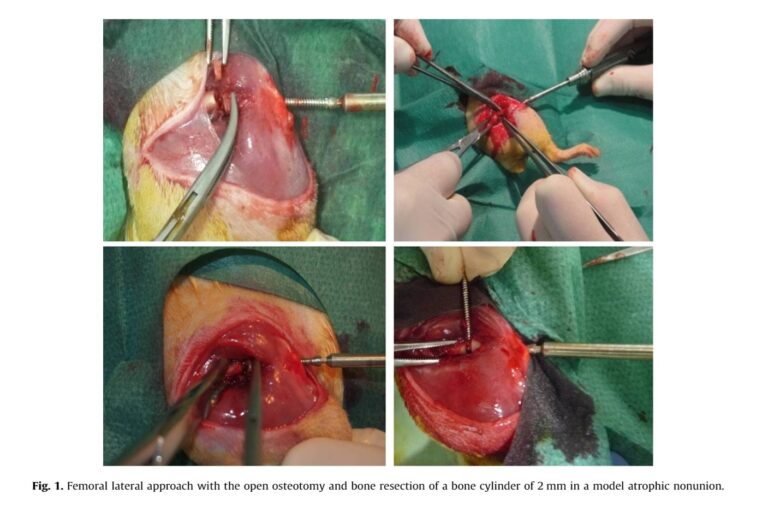
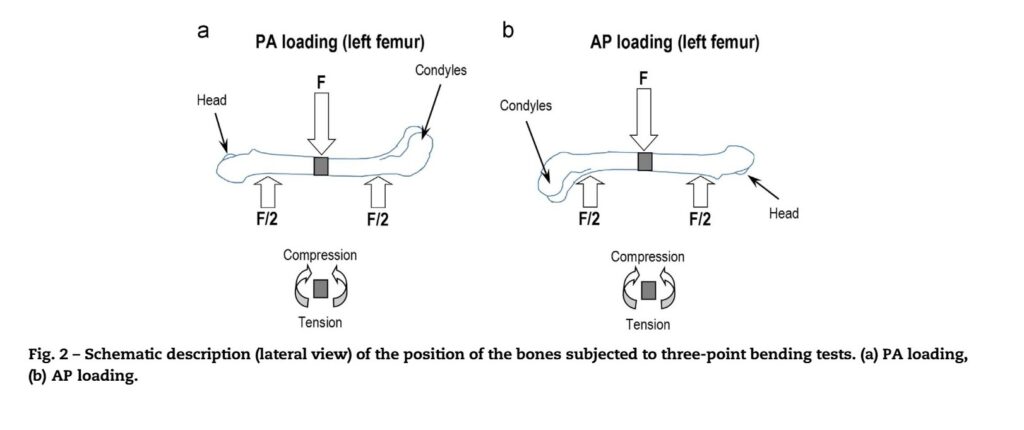
Sin embargo, lo más sorprendente ocurrió cuando los ingenieros de materiales se dieron cuenta de que la ciencia médica llevaba décadas cometiendo un error de cálculo. Al probar la resistencia de un hueso, los laboratorios de todo el mundo solían colocarlo en la máquina en cualquier posición, sin importar qué lado recibía la presión. Los expertos de LADICIM sospecharon que esto era un error, ya que un hueso no es un cilindro perfecto, sino una estructura irregular y asimétrica.
Para explicarlo de forma sencilla: es como intentar doblar una regla de plástico. Si la doblas por la parte plana, es fácil; pero si intentas doblarla de canto, es muchísimo más difícil. El equipo demostró en una investigación de referencia que, dependiendo de si el hueso se apoya por su cara delantera o trasera, los resultados cambian drásticamente [4]. Este despiste geométrico había provocado errores de hasta el 63% en miles de estudios previos en todo el mundo. Gracias a este hallazgo, LADICIM ha establecido un nuevo estándar internacional: ahora, la ciencia sabe que para medir bien la fuerza de un hueso, la orientación lo es todo.
El genoma a través del prisma biomecánico
La sinergia entre ingenieros y médicos ha alcanzado recientemente un nuevo nivel al entrar en el mundo de la genética. El reto es entender por qué, ante una caída similar, el hueso de una persona aguanta y el de otra se quiebra como el cristal. Para ello, el consorcio puso el foco en un gen llamado TP53, conocido en medicina como «el guardián del genoma». Su función normal es vigilar que nuestras células estén sanas; si detecta que una célula está dañada o ha envejecido peligrosamente, ordena su retirada para mantener el equilibrio del tejido.
Sin embargo, los investigadores descubrieron que una pequeña variante en este gen (llamada Arg72Pro) altera drásticamente la calidad del hueso [5]. Al analizar este fenómeno con el MicroTAC, observaron que los ratones con esta variante tienen una estructura interna ósea mucho más débil y porosa. La razón radica en que la mutación debilita los mecanismos de control: el cuerpo fabrica menos frenos naturales contra la destrucción del hueso y, además, favorece la acumulación de células senescentes.
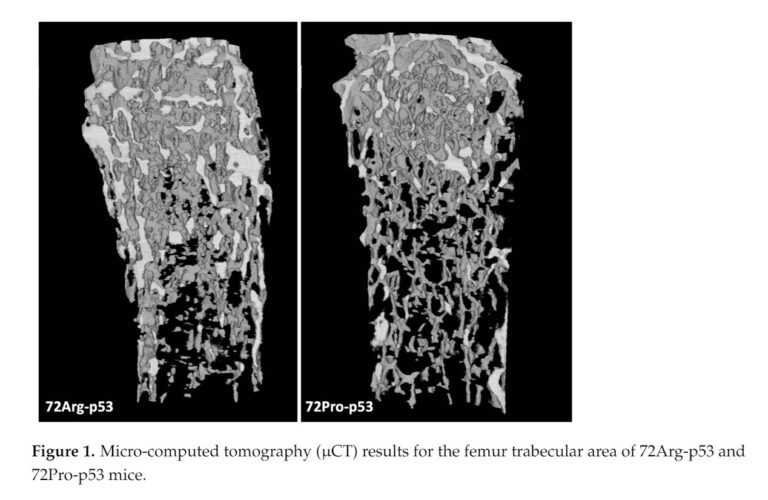
Estas células senescentes son unidades biológicas que han agotado su capacidad de división pero que, en lugar de ser eliminadas, permanecen estancadas en el tejido óseo. Al quedarse instaladas en el hueso sin cumplir su función original, generan una suerte de interferencia química, liberando sustancias que degradan y debilitan toda la estructura desde su interior. «Poder analizar cómo estos cambios genéticos afectan a la resistencia real del hueso nos ha abierto una puerta inmensa», apunta con satisfacción el doctor Riancho.
Esta línea de investigación ha revelado incluso conexiones insospechadas entre nuestras defensas y nuestro esqueleto. En un estudio con modelos inmunodeficientes [6], el equipo descubrió que la salud de los huesos depende de un diálogo constante con nuestro sistema inmunitario y nuestra flora bacteriana. De hecho, observaron que, en ciertos casos, la ausencia de defensas evitaba efectos secundarios graves en la mandíbula tras usar ciertos fármacos. Es decir: la solidez de nuestro esqueleto no es solo una cuestión de calcio, sino el resultado de una compleja red de células, genes y bacterias.
Tecnología intraoperatoria: el futuro a corto plazo
Consolidadas las metodologías en el entorno estático del laboratorio, los investigadores otean ya el horizonte de la práctica clínica real. El desafío imperativo es que la ingeniería baje a la arena del quirófano para guiar la mano del cirujano en tiempo real.
«Esta moderna tecnología permitirá, en un futuro no lejano, disponer de una herramienta que permita al cirujano diagnosticar con seguridad qué cuerdas tendinosas son normales o están afectadas por el proceso degenerativo, aunque aparentemente tengan un aspecto de normalidad», anticipa el doctor Revuelta.
El primer paso ya está en marcha mediante una alianza transversal con el Grupo de Ingeniería Fotónica de la Universidad de Cantabria, dirigido por los profesores José Miguel López Higuera y Olga Conde Portilla. Utilizando la Tomografía de Coherencia Óptica (OCT), planean desarrollar un sensor intraoperatorio del tamaño de un bisturí. El dispositivo, apoyado en los algoritmos de entropía de Shannon previamente calibrados por LADICIM, evaluará los patrones de birrefringencia del colágeno in situ. Bastará un barrido de luz para que el software dicte si el tejido mitral resistirá la presión cardíaca o si debe ser extirpado irremediablemente.
De igual forma, la traumatología persigue sus propios oráculos algorítmicos. «Sería interesante la aplicación de los métodos de aprendizaje automático para una mejor predicción de la resistencia de los huesos, tanto en vivo, a partir de estudios radiológicos y otras técnicas, como en muestras ex vivo», asegura Riancho.

La metamorfosis experimentada por LADICIM a lo largo de las últimas dos décadas ejemplifica a la perfección el valor real de la investigación transversal. Un departamento históricamente centrado en homologar raíles ferroviarios, certificar la fatiga de grandes aceros y validar materiales de construcción, ha sabido volcar su potente herencia matemática y estructural en el complejo puzle del cuerpo humano.
El trayecto compartido por el Laboratorio de la Universidad de Cantabria y las instalaciones de investigación clínica del Hospital Marqués de Valdecilla arroja una lección vital: los grandes saltos tecnológicos nacen en los márgenes y las fricciones entre ciencias aparentemente lejanas. Tratar la degeneración mitral o la osteoporosis con la misma frialdad analítica que exige la construcción de una presa colgante no le resta humanidad a la medicina; por el contrario, dota a los especialistas de herramientas incomparablemente más precisas.
En el corto plazo, este torrente de datos empíricos promete intervenciones cardíacas a medida, recuperaciones traumatológicas mucho más sólidas y una innegable mejora en la calidad de vida de miles de pacientes que, sin saberlo, se benefician del encuentro entre la ingeniería y la biología molecular.
Referencias Científicas
- [1] Casado, J. A., Diego, S., Ferreño, D., Ruiz, E., Carrascal, I., Méndez, D., Revuelta, J. M., Pontón, A., Icardo, J. M., & Gutiérrez-Solana, F. (2012). Determination of the mechanical properties of normal and calcified human mitral chordae tendineae. Journal of the Mechanical Behavior of Biomedical Materials, 13, 1-13.
- [2] Ferreño, D., Revuelta, J. M., Sainz-Aja, J. A., Wert-Carvajal, C., Casado, J. A., Diego, S., Carrascal, I. A., Silva, J., & Gutiérrez-Solana, F. (2022). Shannon entropy as a reliable score to diagnose human fibroelastic degenerative mitral chords: A micro-ct ex-vivo study. Medical Engineering and Physics, 110, 103919.
- [3] Pérez Núñez, M. I., Ferreño Blanco, D., Alfonso Fernández, A., Casado de Prado, J. A., Sánchez Crespo, M., De la Red Gallego, M., … & Riancho Moral, J. A. (2015). Comparative study of the effect of PTH (1-84) and strontium ranelate in an experimental model of atrophic nonunion. Injury, 46, 2359-2367.
- [4] Ferreño, D., Sainz-Aja, J. A., Carrascal, I. A., Diego, S., Ruiz, E., Casado, J. A., Riancho, J. A., Sañudo, C., & Gutiérrez-Solana, F. (2017). Orientation of whole bone samples of small rodents matters during bending tests. Journal of the Mechanical Behavior of Biomedical Materials, 65, 200-212.
- [5] Usategui-Martín, R., Galindo-Cabello, N., Pastor-Idoate, S., Fernández-Gómez, J. M., del Real, Á., Ferreño, D., … & Pérez-Castrillón, J. L. (2024). A Missense Variant in TP53 Could Be a Genetic Biomarker Associated with Bone Tissue Alterations. International Journal of Molecular Sciences, 25(3), 1395.
- [6] del Real, Á., López-Delgado, L., Sañudo, C., García-Montesinos, B., Wert-Carvajal, C., Laguna, E., García-Ibarbia, C., Saiz-Aja, J. A., Ferreño, D., Casado, J. A., Menéndez, G., Pérez-Núñez, M. I., & Riancho, J. A. (2024). Limitations of immunodeficient mice as models for osteoporosis studies. Revista de Osteoporosis y Metabolismo Mineral (ROMM).
Más Noticias

LADICIM aplica la ciencia de los materiales al estudio del patrimonio arqueológico
La Unidad de Arqueometría y Patrimonio colabora desde hace más de 30 años con arqueólogos e investigadores para analizar piezas históricas mediante técnicas avanzadas no

LADICIM lidera los ensayos de durabilidad del hormigón en el proyecto Isobara
La investigación, en la que también participan IHCantabria y Seaplace, busca estandarizar una plataforma flotante de hormigón para energía eólica marina. El proyecto Isobara, que

LADICIM colabora en la guía para implantar en España la normativa europea de hormigón reciclado en estructuras
El objetivo es proporcionar recomendaciones precisas para optimizar el diseño y la ejecución de estructuras con hormigón reciclado, contribuyendo a la transición hacia una construcción
